Частицам (атомам, ионам) присуще стремление к беспорядочному движению, поэтому система стремится перейти из более упорядоченного состояния в менее упорядоченное.
Так, если, например, баллон с газом соединить с сосудом, то газ из баллона будет распределяться по всему объему сосуда. При этом система из более упорядоченного состояния (с меньшим беспорядком) переходит в состояние менее упорядоченное (с большим беспорядком).
Количественной мерой беспорядка является энтропия S.
Или другими словами: энтропия – мера неупорядоченности системы. Ее представляют как логарифмическое выражение вероятности существования вещества или различных его форм:
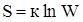 ,
,
где S – энтропия, 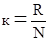 - коэффициент пропорциональности (к – постоянная Больцмана), W – термодинамическая вероятность существования вещества или какой-либо его формы, т.е. число возможных микросостояний, соответствующих данному макросостоянию вещества.
- коэффициент пропорциональности (к – постоянная Больцмана), W – термодинамическая вероятность существования вещества или какой-либо его формы, т.е. число возможных микросостояний, соответствующих данному макросостоянию вещества.
При переходе системы из более упорядоченного состояния в менее упорядоченное энтропия возрастает (DS > 0). Чтобы оценить изменение энтропии при переходе из состояния 1 в состояние 2 необходимо, как обычно, из величины какого-либо свойства, характеризующего конечное состояние, вычесть величину того же свойства, характеризующего начальное состояние:
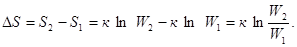
II закон термодинамики: в изолированных системах энтропия самопроизвольно протекающего процесса возрастает, т.е. DS > 0.
Переход же системы из менее упорядоченного состояния в более упорядоченное связан с уменьшением энтропии, и самопроизвольное протекание подобного процесса менее вероятно. Так, ясно, что в рассматриваемом примере невероятно, чтобы газ самостоятельно собрался в баллоне.
В случае перехода системы из менее упорядоченного состояния в более упорядоченное энтропия системы уменьшается (DS < 0).
Нетрудно понять, что энтропия возрастает при переходе жидкости в пар, при растворении кристаллического вещества, при расширении газов и т.д. Во всех этих случаях наблюдается уменьшение порядка в относительном расположении частиц. Наоборот, в процессах конденсации, кристаллизации веществ энтропия уменьшается.
Вероятность существования различных соединений вещества (газ, кристаллическое, жидкое) можно описать как некоторое свойство и количественно выразить значением энтропии S. [Энтропия может измеряться в энтропийных единицах 1 э.е. = 1 кал/(моль×град.) = 4,1868 Дж/моль×град.] Энтропии веществ, как и энтальпии их образования, принято относить к определенным условиям. Обычно это стандартные условия. Энтропию в этом случае обозначают 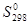 и называют стандартной.
и называют стандартной.
В соответствии со степенью беспорядка энтропия вещества в газовом состоянии значительно выше, чем в жидком, а тем более – в кристаллическом. Например, 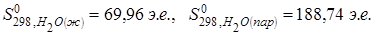
При данном агрегатном состоянии энтропия тем значительнее, чем больше атомов в молекуле. Например,
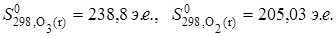 ;
;
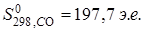
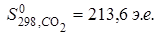
Чем больше твердость вещества, тем меньше его энтропия. Энтропия возрастает с увеличением степени дисперсности частиц вещества.
Для химических реакций в целом
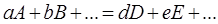
изменение энтропии будет
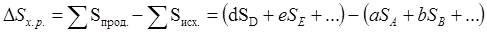 .
.
Об изменении энтропии в химической реакции можно судить по изменению объема в ходе реакции:
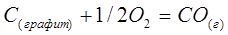 ,
, 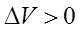 и
и 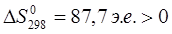 ;
;
Перейти на страницу:
1 2 3 4 5 6 7 8